La massa molare (M) esprime la massa di una mole di particelle. La sua unità di misura è g/mol.
Una mole di particelle contiene 6,022×1023 particelle conosciuto anche come Numero di Avogadro. Il concetto di mole può essere esteso ad atomi, molecole, ioni, composti ionici e altro.
Si può dimostrare che esiste una relazione tra massa molare e numero di massa e tra massa molare e massa atomica eelativa:
- Per un isotopo la massa molare coincide con il numero di massa.
- Per un elemento chimico, costituito da una miscela di isotopi, la massa molare coincide con la massa atomica relativa o peso atomico.
RELAZIONE TRA MASSA MOLARE E NUMERO DI MASSA
Esercizio svolto n.1
Determinale la massa in grammi di una mole dell’isotopo-16 dell’Ossigeno.
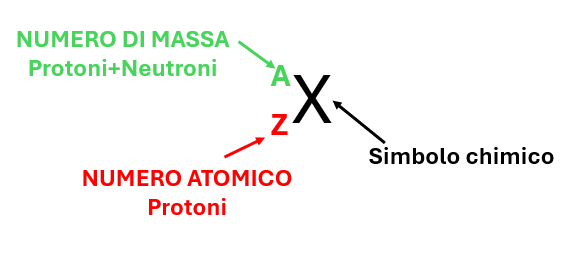
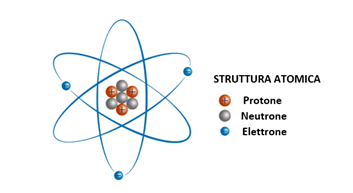
- L’isotopo-16 dell’ossigeno è costituito da 8 protoni, 8 neutroni e 8 elettroni.
- Il Numero Atomico (Z) è pari a 8, mentre il suo numero di massa è pari a 16.
- Per un isotopo il Numero di Massa coincide con la massa atomica in unità di massa atomica (u).
- Una mole di 16O contiene 6,022×1023 atomi di 16O.
- Massa Atomica = 16 u/atomo x 6,022×1023 atomi = 9,63×1024 u.
- Massa 16O = 9,63×1024 u x 1,66×10-24 g/u = 16 g.
- La massa molare di 16O è uguale a 16 g/mol.
Esercizio svolto n.2
Determinale la massa in grammi di una mole dell’isotopo-14 dell’Azoto.
- L’isotopo-14 dell’azoto è costituito da 7 protoni, 7 neutroni e 7 elettroni.
- Il numero atomico (Z) è pari a 7, mentre il suo numero di massa è pari a 14.
- Per un isotopo, il numero di massa coincide con la massa atomica in Unità di Massa Atomica (u).
- Una mole di 14N contiene 6,022×1023 atomi di 14N.
- Massa Atomica = 14 u/atomo x 6,022×1023 atomi = 8,43×1024 u.
- Massa 14N = 8,43×1024 u x 1,66×10-24 g/u = 14 g.
- La massa molare di 14N è uguale a 14 g/mol.
I risultati ottenuti da questi due esercizi sono stati per l’isotopo-16 dell’Ossigeno 16 g/mol, mentre per l’isotopo-14 dell’Azoto 14 g/mol. É pertanto dimostrata la correlazione tra il Numero di Massa dell’isotopo e la Massa Molare espressa in unità di grammi/mole.
La Massa Molare di un isotopo è pari al suo Numero di Massa espresso in unità di g/mol.
LA MASSA MOLARE DI UN ELEMENTO CHIMICO
Un elemento della tavola periodica è costituito da una serie di isotopi che hanno una diversa abbondanza in natura. L’isotopo-12 del carbonio si trova in una percentuale pari al 98,89%, l’isotopo-13 in percentuale pari all’1,11% mentre l’isotopo-14 è presente solo in piccolissime tracce.
Questo si riflette sul calcolo del peso atomico di un elemento, ottenuto dalla media ponderata dei singoli isotopi che lo costituiscono in accordo con la loro abbondanza in natura. Da tale calcolo è possibile ottenere la massa di un elemento della tavola periodica sotto forma di numero decimale.
Si può dimostrare come la massa molare di un elemento sia numericamente uguale alla suo peso atomico espresso in unità di grammi/mole.
DIMOSTRAZIONE:
Determinare la massa in g/mol di una mole dell’elemento cloro (Cl) sapendo che esso è costituito per 75,77% da 35Cl e per un 24,23% da 37Cl.
Per gli isotopi la massa molare coincide con il numero di massa.
35Cl ha una massa molare di 35 g/mol.
37Cl ha una massa molare di 37 g/mol.
Per determinare la massa molare dell’elemento è necessario fare la media ponderata delle masse molari dei singoli isotopi in accordo con la loro abbondanza relativa.
Guardando la tavola periodica, si osserva come il valore numerico della Massa Molare coincida con quella del Peso Atomico. Questo è solitamente riportato sotto il simbolo dell’elemento chimico (Figura 1).

Figura 1 – Valore di massa atomica e di massa molare di un elemento nella tavola periodica
CONCETTI CHIAVE:
- La massa molare esprime la massa in grammi di un numero di Avogadro di particelle.
- La massa molare di una mole di un isotopo è uguale al suo numero di massa espresso in g/mol.
- La massa molare di un elemento della tavola periodica è pari numericamente alla sua massa atomica relativa o peso atomico espressa in unità di g/mol.